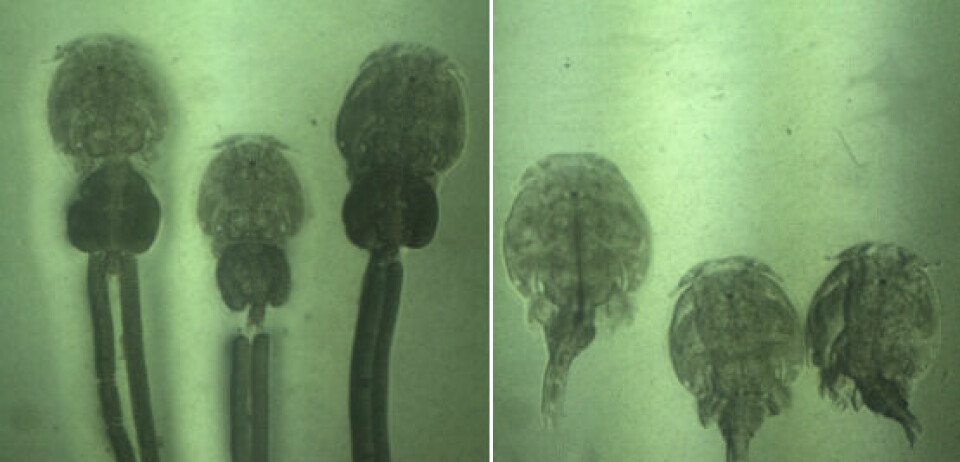
Nuevo modelo de bajo costo para el estudio de infección por Caligus
*Columna de opinión para Salmonexpert del Dr. Jorge Parodi, de LaBCeMA, Universidad Mayor, sede Temuco.
En las últimas semanas, ha retornado el tema de la infección por Caligus rogercresseyi, la caligidosis, una parasitosis que afecta intensamente a la industria del salmón. Los Azametifos han bajado su eficacia, encabezando la caída de los fármacos convencionales, por lo que se están implementando nuevos sistemas.
Hace unos años, dentro del trabajo de tesis de alumnos del laboratorio, vimos el impacto del uso de cultivo en jaulas profundas (Riquelme et al 2017) y diversos aditivos para aumentar el mucus como barrera (Concha et al 2017). En ambas ocasiones, pudimos observar que el foco del control de la caligidosis es el adulto. Durante el 2018, estuvimos trabajando con la industria del salmón en algún sistema para estudiar mejor este parásito, modificando algunas técnicas para estudiar su cinética.
Es así que en el congreso mundial de Caligus, en Punta Arenas, presentamos nuestros resultados, donde se muestra que el foco del control del parásito sigue siendo el adulto.
Nuestros esfuerzos generaron un sistema de bajo costo de análisis cinético, registrando en un sistema de video de alto contraste el movimiento de los copepoditos y luego los analizamos usando un programa de fuente abierta, en esta caso el ImageJ con un adaptador del CASA, para el análisis de partículas. Así, pudimos estimar el porcentaje de formas móviles en las muestras expuestas a diversas moléculas, además de algunos parámetros cinéticos como VSL, VAP y VCL.
De esta forma, pudimos usar estrategias ya conocidas, como el uso de agua corriente o emamectina y evaluar los cambios cinéticos. Ambos compuestos redujeron los movimientos, pero asociados a la muerte de los copepoditos. Sin embargo, nos interesa explorar compuestos subtóxicos, que generen cambios en la función del parásito, en particular su movimiento más que su muerte.
En ese aspecto, recientes estudios han determinado la presencia de receptores a glutamato como el kainato (Núñez-Acuña et al 2014) y que son regulados por dietas y aditivos de éstas en su expresión (Núñez-Acuña 2016) en el parásito, lo que habla de blancos moleculares. Además, diversos trabajos en artrópodos, determinan la importancia de los receptores GABA en la función de ellos (Casida y Durkin, 2015).
Por esto usamos Taurina, un modulador de receptores GABA, glutamato y GABA como moléculas de prueba. Este sistema mostró un efecto reversible sobre la actividad cinética de los parásitos, sugiriendo un efecto fisiológico y no tóxico. Los compuestos pueden alterar la función de movimiento de los copepoditos y alterar la capacidad de infección de los mismos.
Esto reduciría la capacidad del piojo de llegar a su huésped y completar su ciclo, bajando la carga ambiental del mismo. Dichos datos son postulados al próximo congreso de Caligus nacional para ser discutidos con otros investigadores y contaron con el apoyo de SalmoFood, empresa que aportó con moléculas y el acceso al parásito, para las pruebas.
¿Por qué sería importante alterar la función de movimiento de las formas libres? La experiencia con parasitosis en general, es la reducción de la carga ambiental, donde el control de adulto debe ir de la mano de buenas prácticas y reducir la presencia de otros estados del parásito. En el caso de la caligidosis, no se da esto.
Si bien han mejorado las prácticas internas de cultivos, aún no se considera el efecto de la infección de algún barrio y el movimiento de las formas libres en él, por las mareas, viento y el efecto de la temperatura. Los modelos de simulación de las condiciones de los barrios, deben ser un elemento clave para proponer medidas profilácticas frente a la caligidosis.
¿Qué podemos hacer para un control ambiental? Reducir la capacidad del parásito de llegar al huésped, en un formato menos tóxico y más específico. Debemos recordar que este parásito es propio del país, endémico e infecta a peces endémicos, siendo el Róbalo su reservorio natural. Por ende, estrategias que reduzcan que estas formas libres lleguen a los centros de cultivos de salmón e infecten, logrando desarrollar su ciclo y volver a reinfectar, puede ser una nueva mirada.
En ese sentido, diversos grupos en Chile han tomado acento en describir más de la fisiología del parásito. Es así como se logrado secuenciar parte de su material genético e identificar identidades moleculares, receptores, que pueden ser blancos de nuevos desarrollos farmacológicos. Esto es vital para generar herramientas de control aún más novedosas, dirigidas y de bajo impacto ambiental.
Hemos desarrollado un modelo, del que pretendemos presentar sus avances en la próxima reunión de Caligus, tras explorar el efecto de diversas moléculas que puedan reducir el movimiento de las formas libres, su cinética, con el fin de aumentar el tiempo de llegada a los huéspedes y reducir de esta forma el número de ciclos del parásito.
Esto nos invita a pensar que debemos reenfocar el blanco de dónde controlar el parásito, y si bien las formas adultas son más visibles y causan más daño a la industria del salmón, no son el blanco más importante para el control del ciclo de vida de estos ectoparásitos.